pH值
1. 什么是水的pH值?它有什么意义?
pH值是水溶液最重要的理化参数之一。凡涉及水溶液的自然现象,化学变化以及生产过程都与pH值有关,因此,在工业、农业、医学、环保和科研领域都需要测量pH值。
水的pH值是表示水中氢离子活度的负对数值,表示为:
pH= - lg aH+
pH值有时也称氢离子指数,由于氢离子活度的数值勤往往很小,在应用很不方便,所以就用pH值之一概念来作为水溶液酸性、碱性的判断指示。而且,氢离子活度的负对数值能够表示出酸性、碱性的变化幅度的数量级的大小,这样应用起来就十分方便,并由此得到:
⑴中性水溶液,pH= - lg aH+=-lg10-7=7
⑵酸性水溶液,pH<7,pH值越小,表示酸性越强;
⑶碱性水溶液,pH>7,pH值越大,表示碱性越强。
pH标度
pH测量是一种相对测量,它仅仅指示标准溶液与未知溶液之间的pH差别,实际测量时,需要用标准缓冲溶液定期进行校准。因此,为了达到量值的一致,必须建立pH标度。pH标度范围定为0~14pH,pH标度的量值由基准缓冲溶液的pHs值确定。
因此,pH标度的含义可表达为:根据pH定义,在0~14pH范围内选择若干个pH缓冲溶液作为pH标度的固定点,并且采用当代技术能达到的最准确的方法测定它们的pHs值。国际上有二种pH标度,即多种基准pH标度和单种基准pH标度,中国采用多种基准pHs标度。
pH缓冲溶液
pH缓冲溶液是一种能使pH值保持稳定的溶液。如果向这种溶液中加入少量的酸或碱,或者在溶液中的化学反应产生少量的酸或碱,以及将溶液适当稀释,这个溶液的pH值基本上稳定不变,这种能对抗少量酸或碱或稀释,而使pH值不易发生变化的溶液就称为pH缓冲溶液。
pH标准缓冲溶液具有以下特点:
⑴标准溶液的pH值是已知的,并达到规定的准确度。
⑵标准溶液的pH值有良好的复现性和稳定性,具有较大的缓冲容量,较小的稀释值和较小的温度系数。
⑶溶液的制备方法简单。
如何配制pH缓冲溶液?
对于一般的pH测量,可使用成套的pH缓冲试剂(可配制250ml),配制溶液时,应使用去离子水,并预先煮沸15~30分钟,以除去溶解的二氧化碳。剪开塑料袋将试剂倒入烧杯中,用适量去离子水使之溶解,并冲洗包装袋,再倒入250ml容量瓶中,稀释至刻度,充分摇匀即可。
如何正确保存和使用pH缓冲溶液?
缓冲溶液配制后,应装在玻璃瓶或聚乙稀瓶中(碱性的pH缓冲液如pH9.18、pH10.01、pH12.46等,应装在聚乙稀瓶中)瓶盖严密盖紧,在冰箱中低温(5-10℃)保存,一般可使用二个月左右,如发现有混浊、发霉或沉淀等现象,不能继续使用。使用时,应准备几个50ml的聚乙稀小瓶,将大瓶中缓冲溶液倒入小瓶中,并在环境温度下放置1~2小时,等温度平衡后再使用。使用后不得再倒回大瓶中,以免污染,小瓶中的缓冲溶液在>10℃的环境条件下可以使用2~3天,一般pH7.00、pH6.86及pH4.00三种溶液使用时间可以长一些,pH9.18和pH10.01溶液由于吸收空气中的CO2,其pH值比较容易变化.
pH缓冲溶液有何用途?
⑴pH测量前标定校准pH计。
⑵用以检定pH计的准确性,例如用pH6.86和pH4.00标定pH计后,将pH电极插入pH9.18溶液中,检查仪器显示值和标准溶液的pHs值是否一致。
⑶在一般精度测量时检查pH计是否需要重新设定。pH计标定并使用后也许会产生漂移或变化,因此在测试前将电极插入与被测溶液比较接近的标准缓冲液中,根据误差大小确定是否需要重新标定。
⑷检测pH电极的性能。
8. 使用瓶装的pH缓冲溶液有什么优点?
在pH计经销商处一般还有用聚乙稀塑料瓶瓶装的pH标准缓冲溶液销售。它和用pH缓冲试剂自己配制的缓冲溶液比较,由于它其中添加了显色剂和防腐剂,因此不同pH值的缓冲液有不同的颜色,使用时不易搞错,并且在常温下保存不会发霉变质,保存期可长达一年,因此使用特别方便。有pH4.00、pH6.86、pH7.00、pH9.18、pH10.01五种,并有500ml大瓶和50ml小瓶二种规格。
pH电极
实验室和工业型pH电极有什么区别? 从使用上讲,实验室pH电极是在较好的环境条件下进行短时间间断测试;而工业pH电极是在较差的环境条件下进行长期连续的测试。从性能上讲,实验室pH电极要求电极的准确性和重复性要好,响应快;而工业pH电极则要求电极的长期稳定性好。从结构上讲实验室pH电极要求简单轻便,而工业型pH电极则要求结构牢固,要考虑能够安装,并且能抵抗各种电场和磁场的干扰。
pH电极为何要浸泡?如何正确浸泡? pH电极使用前必须浸泡,因为pH球泡是一种特殊的玻璃膜,在玻璃膜表面有一很薄的水合凝胶层,它只有充分湿润的条件下才能与溶液中的H+离子良好的响应。同时,玻璃电极经过浸泡,可以使不对称电势大大下降并趋向稳定。
pH玻璃电极一般可以用蒸馏水或pH4缓冲溶液浸泡。通常使用pH4缓冲液更好一些,浸泡时间8小时至24小时或更长,根据球泡玻璃膜厚度、电极老化程度而不同。同时,参比电极的液接界也需要浸泡。因为如果液接界干涸会使液接界电势增大或不稳定,参比电极的浸泡液必须和参比电极的外参比溶液一致,即3.3mol/LKCl溶液或饱和KCl溶液,浸泡时间一般几小时即可。
因此,对pH复合电极而言,就必须浸泡在含KCl的pH4缓冲液中,这样才能对玻璃球泡和
液接界同时起作用。这里要特别提醒注意,因为过去人使用单支的pH玻璃电极已习惯于用去离子水或pH4缓冲液浸泡,后来使用pH复合电极时依然采用这样的浸泡方法引起的直接后果就是使一支性能良好的pH复合电极变成一支响应慢、精度差的电极,而且浸泡时间越长性能越差,因为经过长时间的浸泡,液接界内部(例如砂芯内部)的KCl浓度已大大降低了,使液接界电势增大和不稳定。当然,只要在正确的浸泡溶液中重新浸泡数小时,电极还是会复原的。
另外,pH电极也不能浸泡在中性或碱性的缓冲溶液中,长期浸泡在此类溶液中会使pH玻璃膜响应迟钝。正确的pH电极浸泡液的配制:取pH4.00缓冲剂(250ml)一包,溶于250ml纯水中,再加入56克分析纯KCl,适当加热,搅拌至完全溶解即成。 pH电极如何清洗? 球泡和液接界污染后先用以下溶剂清洗,再用去离子水洗去溶剂,将电极浸入浸泡液中活化。
污 染 物 清 洗 剂
无机金属氧化物 低于1mol/L稀酸
有机油脂类物 稀洗涤剂(弱酸性)
树脂高分子物质 稀酒精、丙酮、乙醚
蛋白质血球沉淀物 酸性酶溶液(如食母生片)
颜料类物质 稀漂白液、过氧化氢
如何检测pH电极的好坏? 用户可按下表数据自行检测pH电极的好坏,步骤如下(pH计调至mV档)
⑴测试零电位pH值,零点pH值:7±0.5pH pH电极插入pH4.00缓冲液中,稳定后读数(预先测试出溶液的温度)。例如25℃时读数值E1’=186mV(取值),而准确值为178mV(见表格),则误差值=186-178mV,换算成pH值:8/59.16=0.14pH(59.16mV/pH是25℃时的K值,见表格)。因此零点pH值合格。一般新电极零电位误差≤±0.3pH,如零电位误差>±0.5pH,电极的测试误差会比较大,尤其当测试溶液温度变化较大时误差会更大。如果测试精度要求不高,则零电位误差值还可以大一些,但不能超过1pH.
⑵测试电极百分理论余率(PTS)
记录(1)步骤中的测试数据186mV,将电极清洗后再插入pH9.18缓冲液中,稳定后读数,E2’=111mV(取值),ΔE’=E1’+E2’=186+111=297mV,与表格中的ΔE对照,PTS=97%,合格,一般新电极PTS≥97%,使用长久的电极可以放宽一些,但一般应PTS≥95%,除非测试精度要求很低。
⑶将电极清洗后再插入pH4.00缓冲液,将读数与步骤(1)的数据比较,其误差应≤±2mV,否则表示电极重复性较差。
⑷电极的测试读数应该在30-60秒内稳定,否则表示电极响应太慢。
pH指示电极
对溶液中氢离子活度有响应,电极电位随之而变化的电极称为pH指示电极或pH测量电极。pH指示电极有氢电极、锑电极和玻璃电极等几种,但最常用的是玻璃电极。玻璃电极是由玻璃支杆,以及由特殊成份组成的对氢离子敏感的玻璃膜组成。玻璃膜一般呈球泡状,球泡内充入内参比溶液,插入内参比电极(一般用银/氯化银电极),用电极帽封接引出电线,装上插口,就成为一支pH指示电极。市场销售的最常用的pH指示电极是231玻璃pH电极。单独一支pH指示电极是无法进行测量的,它必须和参比电极一起才能测量。
pH复合电极
将pH玻璃电极和参比电极组合在一起的电极就称为pH复合电极。外壳为塑料的就称为塑壳pH复合电极。外壳为玻璃的就称为玻璃pH复合电极。复合电极的优点是合二为一,使用方便。pH复合电极的结构主要由电极球泡、玻璃支持杆、内参比电极、内参比溶液、外壳、外参比电极、外参比溶液、液接界、电极帽、电极导线、插口等组成。
⑴电极球泡:它是由具有氢功能的锂玻璃熔融吹制而成,呈球形,膜厚在0.1~0.2mm左右,电阻值<250兆欧(25℃)。
⑵玻璃支持管:是支持电极球泡的玻璃管体,由电绝缘性优良的铅玻璃制成,其膨胀系数应与电极球泡玻璃一致。
⑶内参比电极:为银/氯化银电极,主要作用是引用电极电位,要求其电位稳定,温度系数小。
⑷内参比溶液:零电位为7pH的内参比溶液,是中性磷酸盐和氯化钾的混合溶液,玻璃电极与参比电极构成电池建立零电位的pH值,主要取决于内参比溶液的pH值及氯离子浓度。
⑸电极塑壳:电极塑壳是支持玻璃电极和液接界,盛放外参比溶液的壳体,由聚碳酸酯塑压成型。
⑹外参比电极:为银/氯化银电极,作用是提供与保持一个固定的参比电势,要求电位稳定,重现性好,温度系数小。
⑺外参比溶液:为3.3mol/L的氯化钾凝胶电解质,不易流失,无需添加。
⑻砂芯液接界:液接界是构通外参比溶液和被测溶液的连接部件,要求渗透量稳定。
⑼电极导线:为低噪音金属屏蔽线,内芯与内参比电极连接,屏蔽层与外参比电极连接。
pH电极具有以下特性:
⑴不对称电势:当电极的内外参比电极,内外参比溶液均相同时,理论上电池电动势应等于零,但实际上总有几毫伏到几十毫伏的电势差存在,这说明玻璃球泡内外二个界面是不对称的,这一电势差就称为不对称电势。不对称电势与球泡吹制的工艺有关,也与使用中球泡表面受侵蚀或沾污有关,实际使用中,可用电计特设的定位调节器消除它。
⑵零电势:pH电极的零电势是指pH测量电池的电势为零时的溶液的pH值。它取决于内参比溶液的pH值及氯离子浓度。若内参比溶液为0.025mol/L的混合磷酸盐溶液,电极的零电势pH值大于或小于电极的零电势pH值时,电极的极性就要发生改变。
⑶内阻:电极的内阻主要由球泡玻璃膜的内阻决定,它取决于玻璃的组成和厚度,阻值一般为几十兆欧。而且随温度下降而按指数式上升(每下降7℃,内阻增加1倍,例如28℃时为50兆欧,则0℃时为800兆欧)。内阻高的电极对电计的输入阻抗及绝缘屏蔽的要求高,因此电极内阻低一些为好。
⑷碱误差和酸误差:当被测溶液的酸度和碱度增大时,电极电势与溶液pH值将偏离线性关系,这种偏差就称为碱误差和酸误差。碱误差是由于在氢离子浓度很低的溶液中,电极膜的响应不仅与氢离子浓度有关,而且与溶液中碱金属离子浓度有关。碱误差使测得的pH值比实际的数值偏低。酸误差在较低的pH范围内(pH<1~2)出现,酸误差使pH测量值比实际数值偏高。
可充式和非可充式pH复合电极有何区别?
pH复合电极外壳有塑料和玻璃的区分。可充式pH复合电极外壳上有一加液孔,当电极的外参比溶液流失后,可将加液孔打开,重新补充KCl溶液。而非可充式pH复合电极内装凝胶状KCl,不易流失也无加液孔。
可充式pH复合电极的特点是参比溶液有较高的渗透速率,液接界电位稳定重现,测量精度较高。而且当参比电极减少或受污染后可以补充或更换KCl溶液,但缺点是使用较麻烦。可充式pH复合电极使用时应将加液孔打开,以增加液体压力,加速电极响应,当电介液液面低于加液孔2cm时,应及时补充新的电介液。
非可充式pH复合电极的特点是维护简单使用方便,因此也得到广泛的应用。但作为实验室pH电极使用时,在长期和连续的使用条件下,液接界处的KCl浓度会减少,影响测试精度。因此非可充式pH复合电极不用时,应浸在电极浸泡液中,这样下次测试时电极性能会很好,而大部分实验室pH电极都不是长期和连续的测试,因此这种结构对精度的影响是比较小的。而工业pH复合电极由于对测试精度的要求比较低,所以使用方便就成为主要的选择。
如何正确使用pH复合电极?
⑴球泡前端不应有气泡,如有气泡应用力甩去。
⑵电极从浸泡瓶中取出后,应在去离子水中晃动并甩干,不要用纸巾擦试球泡,否则由于静电感应电荷转移到玻璃膜上,会延长电势稳定的时间,更好的方法是使用被测溶液冲洗电极。
⑶pH复合电极插入被测溶液后,要搅拌晃动几下再静止放置,这样会加快电极的响应。尤其使用塑壳pH复合电极时,搅拌晃动要厉害一些,因为球泡和塑壳之间会有一个小小的空腔,电极浸入溶液后有时空腔中的气体来不及排除会产生气泡,使球泡或液接界与溶液接触不良,因此必须用力搅拌晃动以排除气泡。
⑷在粘稠性试样中测试之后,电极必须用去离子水反复冲洗多次,以除去粘附在玻璃膜上的试样。有时还需先用其他溶剂洗去试样,再用水洗去溶剂,浸入浸泡液中活化。
⑸避免接触强碱或腐蚀性溶液,如果测试此类溶液,应尽量减少浸入时间,用后仔细清洗干净。
⑹避免在无水乙醇、浓硫酸等脱水性介质中使用,它们会损坏球泡表面的水合凝胶层。
⑺塑壳pH复合电极的外壳材料是聚碳酸酯塑料(PC),PC塑料在有些溶剂中会溶解,如四氯化碳、三氯乙稀、四氢呋喃等,如果测试中含有以上溶剂,就会损坏电极外壳,此时应改用玻璃外壳的pH复合电极。
参比电极
对溶液中氢离子活度无响应,具有已知和恒定的电极电位的电极称为参比电极。参比电极有硫酸亚汞电极、甘汞电极和银/氯化银电极等电极等几种。最常用的是甘汞电极和银/氯化银。参比电极在测量电池中的作用是提供并保持一个固定的参比电势,因此对参比电极的要求是电势稳定、重视,温度系数小,有电流通过时极化电势小。市场销售的常用的参比电极为232参比电极。
不同的参比电极有何区别?
常用的参比电极有甘汞电极和银/氯化银电极二类。甘汞电极具有电势稳定、重现性好的优点,但也有温度滞后性大,不能在高温下使用(<70℃),且电极材料有毒性等缺点。银/氯化银参比电极不仅制备容易,电势稳定,重现性好,而且电极结构牢固,温度滞后性小,当温度变化之后能较快达至新温度下的平衡电势,并且可以在高温下使用。但银/氯化银电极在浓氯化钾溶液中的溶解度较大,因此在电极的外参比溶液中(一般为3.3mol/L氯化钾溶液),应加入氯化银预先饱和,否则参比电极的氯化银镀层会被溶解,使电势不稳定。 毛细管参比电极是银/氯化银参比电极的一种特殊制作形成,它将银/氯化银参比电极烧结在玻璃毛细管中间,将工作介质填充其间。这种参比电极不仅电势稳定,而且可以有效防止因外参比溶液污染而引起的参比电位变化,因此更适合在高温和连续测试的条件下使用。
液接界
什么是液接界?为何要使用高浓度KCI?
在pH测量过程中,均使用参比电极,大多数情况下参比电极带有盐桥溶液。参比电极通过盐桥溶液与被测溶液相连通,这样在被测溶液和参比盐桥溶液之间就形成液接界,液接界两边溶液中的离子不断跨越界面向对面进行扩散,由于各个离子扩散速度不同,而使液接界两边带有符号相反的电荷,产生电位差,即称为液接界电位,也称扩散电位,它会影响电极的测量精度。为了减少液接界的电势差或使其保持稳定及重现,就必须采用高浓度的KCI溶液(≥3.3mol/L)作为电极的外参比盐桥溶液,它有足够高的离子强度,比被测介质的可能的的离子强度还要大5~10倍,因此,在液接界界面上,总是K+和Cl-向外扩散,而由于K+和Cl-的淌度(可以理解成速度)接近相等,正负电荷分布基本均匀,因此形成较小的液接界电势,这就是参比电极中的外参比溶液必须使用高浓度KCI溶液的原因。
液接界有几种结构?它们各有什么特点?
从实际的结构上讲,液接界就是连通电极的外参比溶液(高浓度KCI溶液)与被测溶液的连接部件,这个连接部件的常用结构有陶瓷砂芯、纤维丝、多孔材料(玻璃或塑料)及玻璃磨口等几种。液接界材料的结构要求是能够渗透,但又不能渗透太快,同时又要耐腐蚀,这就是液接界结构的矛盾和困难所在。简单来说就是渗透、耐压、不腐蚀,但又不能渗透太快,同时又要耐腐蚀性好,可以用于高温和高碱溶液;纤维丝结构溶液渗透速度较快,不易堵塞;多孔材料可做成与被测溶液的接触面积较大;最理想的结构应属于玻璃磨口液接界,它可以做成接触面积及渗出速度均较大在,适用于高粘度、浑浊液体及低离子强度液体的测定。
什么是双液接参比电极?它有何优点?
双液接参比电极的结构,有二个液接界和二个参比溶液腔体。
外腔体中一般是KNO3溶液,内腔体中是KCl溶液,它有二个显著的优点:,减少污染,被测溶液只能污染外腔体中的溶液,对内腔体中的KCI溶液影响很小;第二,减少液接界堵塞和离子间的化学反应,例如,若被测溶液中含S-、I-等离子会和参比溶液中的Ag+反应,生成难溶的银化合物堵塞液接界。单支的双液接参比电极有市售,型号为217型甘汞电极。双液接参比电极较多用于工业pH电极。
如何选购pH计|酸度仪|酸度计?应注意五大点。
我们在选购酸度仪时,首先要考虑应用场合,选择笔式pH计,便携式酸度仪,台式酸度计或是工业用pH计;其次是考虑测量需要的精度,选择合适自己使用的精度. BpH-200A型pH计广泛应用于工业、电力、农业、医药、食品、科研和环保等领域。该仪器也是食品厂、饮用水厂办QS、HACCP认证中的必备检验设备。
我们在选购酸度计时需要考虑以下几点:
1.根据应用场合分类可分为:笔式pH计、便携式pH计、实验室pH计和工业pH计等。笔式pH计主要用于代替pH试纸的功能,具有精度低、使用方便的特点。
便携式pH计主要用于现场和野外测方式,要求较高的精度和完善的功能。
实验室pH计是一种台式高精度分析仪表,要求精度高、功能全,包括打印输出、数据处理等等。
工业pH计是用于工业流程的连续测量,不仅要有测量显示功能,还要有报警和控制功能,以及安 装、清洗、抗干扰等等问题的考虑。
2.据pH计仪器精度分类:可分为0.2级、0.1级、0.05级、0.01级,数字越小,精度越高。
3.根据元器件类型分类:可分为晶体管式、集成电路式和单片机微电脑式,更多的是应用微电脑芯片,大大减少了仪器体积和单机成本;但芯片的开发成本很贵
4根据读数指示分类:可分为指针式和数字显示式二种。指针式pH计已很少使用,但指针式仪表能够显示数据的连续变化过程,因此在滴定分析中还有使用。
5.看pH计有没有附带功能,比方说带标配RS232接口,还有一个很重的是温度补偿是自动
还是手动,自动温度补偿的pH计要比手动温度补偿的pH计要方便些,二者之间的价格你就明白了吧。
备注:pH计|酸度仪|酸度计这三个名称意思都一样,只是各地方或者厂家说法不一样
pH计的安装方式有流通式和浸入式两种。
污水处理厂一般选用的是浸入式安装,如该污水处理厂的pH计安装在沉砂池的出口溢流槽内,此处的pH值较具有代表性,且水流平稳,对pH计不会造成大的冲击。定期的维护有助于仪表的准确测量和延长仪表的使用寿命。应当注意传感器和变送器之间的专用电缆不能受潮,否则电极的高阻低压信号将无法传送至变送器。
若电极不测量时,应将黄色保护套管套上,它能使电极处于湿润状态,有利于延长电极的使用寿命。每隔一个月左右,应对电极进行清洗,先用柔和的水流喷洗附着物,再将电极浸泡于清洗液中一段时间,而后用清水洗净。
传感器支架也应清洗。每次清洗之后,要用缓冲剂溶液进行标定,生产厂家一般提供两瓶标准溶液,一瓶pH值等于7,用于标定仪表零点;一瓶pH值等于4,用于标定仪表的信号输出斜率。
保养
1、 pH玻璃电极的贮存
短期:贮存在pH=4的缓冲溶液中;
长期:贮存在pH=7的缓冲溶液中。
2、 pH玻璃电极的清洗
玻璃电极球泡受污染可能使电极响应时间加长。可用CCl4或皂液揩去污物,然后浸入蒸馏水一昼夜后继续使用。污染严重时,可用5%HF溶液浸10~20分钟,立即用水冲洗干净,然后浸入0.1N HCl溶液一昼夜后继续使用。
3、 玻璃电极老化的处理
玻璃电极的老化与胶层结构渐进变化有关。旧电极响应迟缓,膜电阻高,斜率低。用氢氟酸浸蚀掉外层胶层,经常能改善电极性能。若能用此法定期清除内外层胶层,则电极的寿命几乎是无限的。
4、 参比电极的贮存
银-氯化银电极的贮存液是饱和氯化钾溶液,高浓度氯化钾溶液可以防止氯化银在液接界处沉淀,并维持液接界处于工作状态。此方法也适用于复合电极的贮存。
5、 参比电极的再生
参比电极发生的问题绝大多数是由液接界堵塞引起的,可用下列方法解决:
(1) 浸泡液接界:用10%饱和氯化钾溶液和90%蒸馏水的混合液,加热至60~70℃,将电极浸入约5cm,浸泡20分钟至1小时。此法可溶去电极端部的结晶。
(2) 氨浸泡:当液接界被氯化银堵塞时可用浓氨水浸除。具体方法是将电极内充洗净,液放空后浸入氨水中10~20分钟,但不要让氨水进入电极内部。取出电极用蒸馏水洗净,重新加入内充液后继续使用。
(3) 真空方法:将软管套住参比电极液接界,使用水流吸气泵,抽吸部分内充液穿过液接界,除去机械堵塞物。
(4) 煮沸液接界:银-氯化银参比电极的液接界浸入沸水中10~20秒。注意,下一次煮沸前,应将电极冷却到室温。
(5) 当以上方法均无效时,可采用砂纸研磨的机械方法去除堵塞。此法可能会使研磨下的砂粒塞入液接界。造成性堵塞。
维护
实验室使用的电极都是复合电极,其优点是使用方便,不受氧化性或还原性物质的影响,且平衡速度较快。使用时,将电极加液口上所套的橡胶套和下端的橡皮套全取下,以保持电极内氯化钾溶液的液压差。下面就把电极的使用与维护简单作一介绍:
⒈复合电极不用时,可充分浸泡3M氯化钾溶液中。切忌用洗涤液或其他吸水性试剂浸洗。
⒉使用前,检查玻璃电极前端的球泡。正常情况下,电极应该透明而无裂纹;球泡内要充满溶液,不能有气泡存在。
⒊测量浓度较大的溶液时,尽量缩短测量时间,用后仔细清洗,防止被测液粘附在电极上而污染电极。
⒋清洗电极后,不要用滤纸擦拭玻璃膜,而应用滤纸吸干, 避免损坏玻璃薄膜、防止交叉污染,影响测量精度。
⒌测量中注意电极的银—氯化银内参比电极应浸入到球泡内氯化物缓冲溶液中,避免电计显示部分出现数字乱跳现象。使用时,注意将电极轻轻甩几下。
⒍电极不能用于强酸、强碱或其他腐蚀性溶液。
⒎严禁在脱水性介质如无水乙醇、重铬酸钾等中使用。
1、 pH玻璃电极的贮存
短期:贮存在pH=4的缓冲溶液中;
长期:贮存在pH=7的缓冲溶液中。
2、 pH玻璃电极的清洗
在进行操作前,应首先检查电极的完好性。甘汞电极。由于复合电极使用比较广泛,以下主要讨论复合电极。
实验室使用的复合电极主要有全封闭型和非封闭型两种,全封闭型比较少,主要是以国外企业生产为主。复合电极使用前首先检查玻璃球泡是否有裂痕、破碎,如果没有,用pH缓冲溶液进行两点标定时,定位与斜率按钮均可调节到对应的pH值时,一般认为可以使用,否则可按使用说明书进行电极活化处理。活化方法是在4%氟化氢溶液中浸3~5 s左右,取出用蒸馏水进行冲洗,然后在0.1mol/L的盐酸溶液中浸泡数小时后,用蒸馏水冲洗干净,再进行标定,即用pH值为6.86(25℃)的缓冲溶液进行定位,调节好后任意选择另一种pH缓冲溶液进行斜率调节,如无法调节到,则需更换电极。非封闭型复合电极,里面要加外参比溶液即3 mol/L氯化钾溶液,所以必须检查电极里的氯化钾溶液是否在1/3以上,如果不到,需添加3 mol/L氯化钾溶液。如果氯化钾溶液超出小孔位置,则把多余的氯化钾溶液甩掉,使溶液位于小孔下面,并检查溶液中是否有气泡,如有气泡要轻弹电极,把气泡完全赶出。
在使用过程中应把电极上面的橡皮剥下,使小孔露在外面,否则在进行分析时,会产生负压,导致氯化钾溶液不能顺利通过玻璃球泡与被测溶液进行离子交换,会使测量数据不准确。测量完成后应把橡皮复原,封住小孔。电极经蒸馏水清洗后,应浸泡在3 mol/L氯化钾溶液中,以保持电极球泡的湿润,如果电极使用前发现保护液已流失,则应在3 mol/L氯化钾溶液中浸泡数小时,以使电极达到的测量状态。在实际使用时,发现有的分析人员把复合电极当作玻璃电极来处理,放在蒸馏水中长时间浸泡,这是不正确的,这会使复合电极内的氯化钾溶液浓度大大降低,导致在测量时电极反应不灵敏,最终导致测量数据不准确,因此不应把复合电极长时间浸泡在蒸馏水中。
电极使用
1、玻璃电极插座应保持干燥、清洁,严禁接触酸雾、盐雾等有害气体,严禁沾上水溶液,保证仪器的高输入阻抗。
2、 不进行测量时,应将输入短路,以免损坏仪器。
3、 新电极或久置不用的电极在使用前,必须在蒸馏水中浸泡数小时。使电极不对称电位降低达到稳定,降低电极内阻。
4、 测量时,电极球泡应全部浸入被测溶液中。
5、 使用时,应使内参比电极浸在内参比溶液中,不要让内参比溶液倒向电极帽一端,使内参比悬空。
6、 使用时,应拔去参比电极电解液加液口的橡皮塞,以使参比电解液(盐桥)借重力作用维持一定流速渗透并与被测溶液相通。否则,会造成读数漂移。
7、 氯化钾溶液中应该没有气泡,以免使测量回路断开。
8、 应该经常添加氯化钾盐桥溶液,保持液面高于银/氯化银丝。
校准溶液
pH测量一定要标定校准吗?
pH测量通常有比色法(pH试纸或比色皿)和电极法二种。比色法当然不要标定,而电极法就一定要标定,因为电极法pH测量就是将未知溶液与已知pHs值的标准溶液在测量电池中作用比较测定,这是电极法pH测量的“操作定义”所决定的。
pH计因电计设计的不同而类型很多,其操作步骤各有不同,因而pH计的操作应严格按照其使用说明书正确进行。在具体操作中,校准是pH计使用操作中的一重要步骤。表1的数据是精度为0.01级、经过计量检定合格的pH计在未校准时与校准后的测量值,从中可以看出校准的重要性。
尽管pH计种类很多,但其校准方法均采用两点校准法,即选择两种标准缓冲液:一种是pH7标准缓冲液,第二种是pH9标准缓冲液或pH4标准缓冲液。先用pH7标准缓冲液对电计进行定位,再根据待测溶液的酸碱性选择第二种标准缓冲液。如果待测溶液呈酸性,则选用pH4标准缓冲液;如果待测溶液呈碱性,则选用pH9标准缓冲液。若是手动调节的pH计,应在两种标准缓冲液之间反复操作几次,直至不需再调节其零点和定位(斜率)旋钮,pH计即可准确显示两种标准缓冲液pH值。则校准过程结束。此后,在测量过程中零点和定位旋钮就不应再动。若是智能式pH计,则不需反复调节,因为其内部已贮存几种标准缓冲液的pH值可供选择、而且可以自动识别并自动校准。但要注意标准缓冲液选择及其配制的准确性。智能式0.01级pH计一般内存有三至五种标准缓冲液pH值,如科立龙公司的KL-016型pH计等。
其次,在校准前应特别注意待测溶液的温度。以便正确选择标准缓冲液,并调节电计面板上的温度补偿旋钮,使其与待测溶液的温度一致。不同的温度下,标准缓冲溶液的pH值是不一样的。
校准工作结束后,对使用频繁的pH计一般在48小时内仪器不需再次定标。如遇到下列情况之一,仪器则需要重新标定:
⑴溶液温度与定标温度有较大的差异时.
⑵电极在空气中暴露过久,如半小时以上时.
⑶定位或斜率调节器被误动;
⑷测量过酸(pH<2)或过碱(pH>12)的溶液后;
⑸换过电极后;
⑹当所测溶液的pH值不在两点定标时所选溶液的中间,且距7pH又较远时。
1、 测量时应按说明书规定的时间周期对仪器进行校准。
2、 校准时应注意:
标准缓冲溶液温度尽量与被测溶液温度接近。
定位标准缓冲溶液应尽量接近被测溶液的pH值。或两点标定时,应尽量使被测溶液的pH值在两个标准缓冲溶液的区间内。
校准后,应将浸入标准缓冲溶液的电极用水特别冲洗,因为缓冲溶液的缓冲作用,带入被测溶液后,造成测量误差。
3、 记录被测溶液的pH值时应同时记录被测溶液的温度值,因为离开温度值,pH值几乎毫无意义。尽管大多数pH计都具有温度补偿功能,但仅仅是补偿电极的响应而已,也就是说只是半补偿,而没有同时对被测溶液进行温度补偿,即,全补偿。
避免反应
如何避免被测溶液与盐桥成分反应?
如果被测溶液含有可溶性银盐、一价汞盐或铊盐时,盐桥内不能利用氯化钾溶液,而应该用饱和硝酸钾或硝酸铵溶液方能获得满意的测量结果。对非水溶液则应用碘化钠的甲醇溶液和硫氰化钾的乙醇溶液为中间溶液。
总之,不能使盐桥溶液中的成分与被测溶液发生沉淀、氧化还原反应等现象,不然会干扰电动势测定。
如双液接参比电极在测Cl浓度中的应用。
关于pH计的常见信号显示仪表 ProtEX RT6820......模拟信号输入型/积算型显示仪表输入信号 4~20mA, Loop-Power回路供电电压降幅 2.8V, (带背光时5.8V)支持线性的、平方根的或可编程的数学运算Loop-Power回路供电 或 DC供电背光可选 ProtEX RT6830.....脉冲信号输入型/积算型显示仪表电池供电, DC供电, 或输出回路供电电池供电, DC供电, 或输出回路供电 背光可选 ProtEX_Lite PD663 防爆型回路供电过程显示仪表输入信号 4~20mA电压降幅 1.7V, (带背光时4.9V)3-1/2+LCDS数字,0.6”高回路供电背光可选快捷的四键编程问题
pH计的用途
pH计广泛用于净水、自来水、生活用水及各种液体的酸碱度测试。pH值在7.0为中性,7.0以下为酸性,7.0以上为碱性。
随着科学研究的发展和生产技术的进步水分的定量分析已被列为各类物质理化分析的基本项目之一,作为各类物质的一项重要的质量指标。
根据不同形式试样中的不同水分含量提出了测定水分的不同要求。水分测定可以是工业生产的控制分析,也可是工农业产品的质量签定;可以从成吨计的产品中测定含水量等等。
酸度计的级别和仪器的准确度是不同的两个概念,仪器级别与其准确度并不完全一致。酸度计的级别是按其指示器(简称电计)的分度值(分辨率或最小显示值)表示的,例如:分度为0.1pH的仪器称为0.1级仪器;最小显示值为0.001pH的仪器称为0.001级仪器,等等。而仪器的准确度是电计与电极配套测试标准溶液的综合误差,它不仅与电计有关,而且与玻璃电极和参比电极更有关。从实际使用要求出发,电计的分度值为0.1~0.001pH,如果有必要的话,依当前的科技水平,完全可以制作出更精密的电计。但是,由于结构和制造等方面的原因,常用电极的性能还不能达到完全理想的程度。玻璃电极的重复性误差和参比电极的溶液接界电势稳定性都不优于0.01pH。因此,电计的分辨率再高,仪器测试准确度都难优于0.01pH。但是,选择高分辨率的仪器可以限度地克服或消除电计对测试误差的影响。由于要使电计达到满意的精度已不成问题,所以都在仪器的智能化,人性化,可靠性,操作简便以及性价比等方面不断创新和提高。酸度计的级别与其测试准确度的关系在酸度计国家计量检定规程(JJG119-84)中规定如下:
PH酸度计仪器的级别0.2级0.1级0.02级0.01级0.001级
分度值或最小显示值(pH)0.20.10.020.010.001
电计示值误差(pH)±0.1±0.05±0.01±0.01±0.002
配套测试示值总误差(pH)±0.2±0.1±0.02±0.02±0.01
注:配套测试时的测试范围应控制在pH3~pH10内。从上表可以看出,对于0.01级以下的酸度计,示值总误差数值等于其级别,对于0.01级的酸度计,示值总误差为0.02pH,对于0.001级酸度计,其示值总误差也只能达到±0.01pH,而且此时需要使用一级pH标准物质才能得到保证。(注意:pH国家标准物质分一级和二级两种,一般酸度计常用的是二级pH标准物质。)
人们根据生产与生活的需要,科学地研究生产了许多型号的酸度计:
按测量精度
可分0.2级、0.1级、0.01级或更高精度。
按仪器体积
分为笔式(迷你型)、便携式、台式还有在线连续监控测量的在线式。
根据使用的要求
笔式(迷你型)与便携式pH酸碱度计一般是检测人员带到现场检测使用。
选择pH酸碱度计的精度级别是根据用户测量所需的精度决定,而后根据用户方便使用而选择各式形状的pH计。
◆按便携性分的,分为:便携式pH计,台式pH计和笔式pH计。
◆按用途分为:实验室用pH计,工业在线pH计等。
◆按先进程度分为经济型pH计,智能型pH计,精密型pH计或分为指针式pH计,数显式pH计。
◆笔式pH计,一般制成单一量程,测量范围狭,为专用简便仪器。
便携式和台式pH计测量范围较广,常用仪器,不同点是便携式采用直流供电,可携带到现场。实验室pH计测量范围广、功能多、测量精度高。
工业用pH计的特点是要求稳定性好、工作可靠,有一定的测量精度、环境适应能力强、抗干扰能力强,具有模拟里量输出、数字通讯、上下限报警和控制功能等。
什么是pH?pH是拉丁文“Pondus hydrogenii”一词的缩写(Pondus=压强、压力hydrogenium=氢),用来量度物质中氢离子的活性。这一活性直接关系到水溶液的酸性、中性和碱性。水在化学上是中性的,但不是没有离子,即使化学纯水也有微量被离解:严格地讲,在与水分子水合作用以前,氢核不是以自由态存在。
H2O+ H2O=H3O+ + OHˉ,由于水合氢离子(H3O+)的浓度是与氢离子(H+)浓度等同看待,上式可以简化成下述常用的形式:
H2O=H+ + OHˉ
此处正的氢离子,人们在化学中表示为“H+离子”或“氢核”。水合氢核表示为“水合氢离子”。负的氢氧根离子称为“氢氧化物离子”。
利用质量作用定律,对于纯水的离解可以找到一平衡常数加以表示:
K=H3O+×OH-————H2O
由于水只有极少量被离解,因此水的质量摩尔浓度实际为一常数,并且有平衡常数K可求出水的离子积KW。
KW=K×H2O KW= H3O+·OH-=10-7·10-7=10-14mol/l(25℃)
也就是说对于一升纯水在25℃时存在10-7摩尔H3O+离子和10-7摩尔OHˉ离子。
在中性溶液中,氢离子H+和氢氧根离子OHˉ的浓度都是10-7mol/l。如:
假如有过量的氢离子H+,则溶液呈酸性。酸是能使水溶液中的氢离子H+游离的物质。同样,如果使OHˉ离子游离,那么溶液就是碱性的。所以,给出H+值就足以表示溶液的特性,呈酸性还是碱性,为了免于用此分子浓度负冥指数进行运算,生物学家泽伦森(Soernsen)在1909年建议将此不便使用的数值用对数代替,并定义为“pH值”。数学上定义pH值为氢离子浓度的常用对数负值。即pH=-log[H+]。
因此,pH值是离子浓度以10为底的对数的负数:
改变50m3的水的pH值,从pH2到pH3需要500L漂白剂。然而,从pH6到pH7只需要50L的漂白剂。
测量pH值的方法很多,主要有化学分析法、试纸法、电位法。现主要介绍电位法测得pH值。
电位分析法所用的电极被称为原电池。原电池是一个系统,它的作用是使化学反应能量转成为电能。此电池的电压被称为电动势(EMF)。此电动势(EMF)由二个半电池构成,其中一个半电池称作指示电极,它的电位与特定的离子活度有关,如H+;另一个半电池为参比半电池,通常称作参比电极,它一般是测量溶液相通,并且与测量仪表相连。
例如,一支电极由一根插在含有银离子的盐溶液中的一根银导线制成,在导线和溶液的界面处,由于金属和盐溶液二种物相中银离子的不同活度,形成离子的充电过程,并形成一定的电位差。失去电子的银离子进溶液。当没有施加外电流进行反充电,也就是说没有电流的话,这一过程最终会达到一个平衡。在这种平衡状态下存在的电压被称为半电池电位或电极电位。这种(如上所述)由金属和含有此金属离子的溶液组成的电极被称为类电极。
此电位的测量是相对一个电位与盐溶液的成分无关的参比电极进行的。这种具有独立电位的参比电极也被称为第二电极。对于此类电极,金属导线都是覆盖一层此种金属的微溶性盐(如:Ag/Agcl),并且插入含有此种金属盐阴离子的电解质溶液中。此时半电池电位或电极电位的大小取决于此种阴离子的活度。
此二种电极之间的电压遵循能斯特(NERNST)公式:
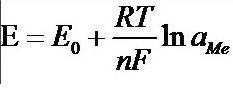
式中:E—电位
E0—电极的标准电压
R—气体常数(8.31439焦耳/摩尔和℃)
T—开氏温度(例:20℃相当于(273.15+20)293.15开尔文)
F—法拉弟常数(96493库化/当量)
n—被测离子的化合价(银=1,氢=1)
ln(aMe)—离子活度aMe的对数
标准氢电极是所有电位测量的参比点。标准氢电极是一根铂丝,用电解的方法镀(涂覆)上氯化铂,并且在四周充入氢气(固定压力为1013hpa)构成的。
将此电极浸入在25℃时H3O+离子含量为1mol/l溶液中便形成电化学中所有电位测量所参照的半电池电位或电极电位。其中氢电极作为参比电极在实践中很难实现,于是使用第二类电极做为参比电极。其中最常用的便是银/氯化银电极。该电极通过溶解的AgCl对于氯离子浓度的变化起反应。
此参比电极的电极电位通过饱和的kcl贮池(如:3mol/l kcl)来实现恒定。液体或凝胶形式的电解质溶液通过隔膜与被测溶液相连通。
利用上述的电极组合—银电极和Ag/AgCl参比电极可以测量胶片冲洗液中的银离子含量。也可以将银电极换成铂或金电极进行氧化还原电位的测量。例如:某种金属离子的氧化阶段。
最常用的pH指示电极是玻璃电极。它是一支端部吹成泡状的对于pH敏感的玻璃膜的玻璃。管内充填有含饱和AgCl的3mol/l kcl缓冲溶液,pH值为7。存在于玻璃膜二面的反映pH值的电位差用Ag/AgCl传导系统,如第二电极,导出。pH复合电极和pH固态电极,此电位差遵循能斯特公式:
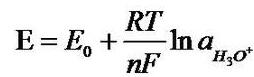
将E0、R、T(298.15K即25℃)等数值代入上式既得:
E=59.16mv/25℃ per pH (式中已将ln(H3O+)转化为pH)
式中R和F为常数,n为化合价,每种离子都有其固定的值。对于氢离子来讲n=1。温度“T”做为变量,在能斯特公式中起很大作用。随着温度的上升,电位值将随之增大。
对于每1℃的温度变大,将引起电位0.2mv/per pH变化。用pH值来表示则每1℃第1pH变化0.0033pH值。
这也就是说:对于20~30℃之间和7pH左右的测量不需要对温度变化进行补偿;而对于温度>30℃或<20℃和pH值>8pH或6pH的应用场合则必须对温度变化进行补偿。
工业PH计,是一种常用的工业仪器设备,主要用来精密测量液体介质的酸碱度值。以及安装、清洗、抗干扰等等问题的考虑。
(1)在实验室配制合适的PH标准液PH4.01PH6.86或PH9.18任选两种,根据现场水样的波动范围选择标准液。如果现场水质经常偏酸性,则选PH4.01、PH6.86两种标样;如果现场水质经常偏碱性,则选PH6.86、PH9.18两种标样。
(2)将传感器从现场取出,用清水清洗探头的玻璃电极。
(3)将两种标准液分别倒入准备好的两个烧杯中。
(4)将电极浸入种标准液中,打开仪表菜单,校准点.不同品牌仪表,校验菜单的操作方法不同,根据随机说明书进行操作。
(5)点校准通过后,用清水冲洗电极,再将电极放入第二种标准液中,翻动仪表菜单,校准第二点。
(6)两点校准完成后,不同品牌的仪表会以不同的方式显示仪表是否通过校验或是否合格。
(7)如果通过,将电极放回被测液体中,使仪表投入运行。
(8)如果仪表校准失败,再重复上述过程校准一遍,如果还不能通过,则更换pH电极。pH电极寿命一般在两年左右。
工业pH计
采用pH计能更好地控制化学反应,达到提高生产率和产品质量以及安全生产的目的。带有自动记录的pH测量系统还可对污染公害提供诉讼的证据。某些间歇生产过程(例如某些化肥生产、食品加工过程)采用pH计后可变为连续生产方式。在现代工业中采用pH计比其他类型的连续分析仪表的总和还多。几乎凡需用水的生产部门都需要采用pH计。其应用范围从工业用水和废物处理到采矿中的浮选过程,包括纸浆和造纸、金属加工、化工、石油、合成橡胶生产、发电厂、制药、食品加工等广泛领域。
不同的pH敏感玻璃膜有何区别?
从形状上看,pH敏感玻璃膜可以制作成球形、圆柱形、平面形和尖锥形等各种不同的外形,主要是为了和被测介质的形态吻合。如球形和圆柱形,主要用于液体介质;平面形主要用于含水的半固体介质,如皮肤、肉类、皮革、纸张等;尖锥形主要用于刺入介质内部测量,如土壤、水果等。从成分组成看区别就更大了,有用于常规使用的敏感玻璃膜,有用于高温使用的敏感玻璃膜,有用于强酸或强碱使用的敏感玻璃膜,有用于高温蒸汽消毒(130℃)的敏感玻璃膜,以及用于低温和低离子强度的敏感玻璃膜等等。有些pH测试不准确或不稳定与pH敏感玻璃膜的选择不当有很大关系。







 编辑
编辑

